1 Denges epidēmijas fons: pieaugoša globāla sabiedrības veselības problēma
Denges drudzis ir akūta odu pārnēsāta vīrusu slimība, ko izraisa denges vīruss (DENV), kas ir kļuvusi par visstraujāk izplatītāko arbovīrusu slimību pasaulē, radot būtiskus draudus sabiedrības veselības drošībai. Pēdējo divu desmitgažu laikā denges drudža saslimstība pasaulē ir dramatiski palielinājusies, un ziņoto gadījumu skaits kopš 2021. gada katru gadu dubultojas [1]. 2023. gada decembrī Pasaules Veselības organizācija (PVO) izsludināja globālu denges drudža ārkārtas stāvokli, lai stiprinātu koordinētus starptautiskos reaģēšanas centienus. PVO epidemioloģiskās aplēses liecina, ka aptuveni 3,9 miljardi cilvēku visā pasaulē ir pakļauti denges infekcijas riskam, un tiek lēsts, ka katru gadu notiek 390 miljoni inficēšanās gadījumu, no kuriem 96 miljoni ir klīniski redzami gadījumi [1,2].
2 epidemioloģiskie svarīgākie notikumi
Denges drudža epidemioloģiskās īpašības veido virusoloģisko faktoru, vektoru ekoloģijas, saimnieka imūnreakciju un sociāli vides apstākļu mijiedarbība. Visaptveroša izpratne par šīm īpašībām ir būtiska efektīvu profilakses un kontroles stratēģiju, kā arī precīzu diagnostikas pieeju izstrādei.
2.1 Pārneses vektori un pārneses modeļi pilsētās
Denges vīruss galvenokārt tiek pārnests arAedes aegypti un Aedes albopictusodi. Starp šīm vektoru sugām Aedes aegypti tiek atzīta par viskritiskāko pārneses vektoru, kam raksturīga augsta “cilvēka pielāgošanās spēja” un plaša izplatība tropu un subtropu pilsētvidē. Atšķirībā no citiem arbovīrusu patogēnu odu vektoriem, Aedes aegypti izrāda šādas galvenās epidemioloģiskās īpašības:
Priekšroka vairošanai antropogēnā vidē (piemēram, ūdens uzglabāšanas konteineros, nolietotās riepās)
-Spēcīgs tropisms cilvēka asinīm kā barības vielu avotam
-Dienas barošanas paradumi
Šīs pazīmes raksturo denges drudzi kā tipisku"Pilsētas infekcijas slimība"ar ievērojami paaugstinātu pārneses efektivitāti blīvi apdzīvotās vietās. Ar PVO saistīti pētījumi ir parādījuši, ka blīvi apdzīvotās pilsētu vidē palielināts odu un cilvēku kontakta biežums var ievērojami paaugstināt DENV pamata reprodukcijas skaitli (R₀), tādējādi paātrinot epidēmiju izplatību [2].
2.2 Globālās izplatības tendences un to virzošie faktori
Saskaņā ar PVO ziņojumiem, pēdējo divu desmitgažu laikā pasaulē ziņoto denges drudža gadījumu skaits ir eksponenciāli pieaudzis [1,3]. Šo augšupejošo tendenci galvenokārt nosaka šādi savstarpēji saistīti faktori:
(1) Klimata pārmaiņas: Pieaugošā globālā temperatūra ne tikai paplašina odu vektoriem piemēroto dzīvotņu ģeogrāfisko diapazonu, bet arī saīsina DENV ārējo inkubācijas periodu odu saimniekorganismā, tādējādi uzlabojot pārneses efektivitāti. PVO ir apstiprinājusi klimata izraisītās odu blīvuma izmaiņas kā uzticamu denges drudža uzliesmojumu telpiski dinamisko dinamikas prognozētāju.
(2) Urbanizācija: strauja un neplānota pilsētu paplašināšanās ir radījusi bagātīgas odu pārnēsātāju vairošanās vietas, savukārt palielinātais iedzīvotāju blīvums ir stiprinājis DENV pārneses ķēžu nepārtrauktību.
(3) Globālā iedzīvotāju pārvietošanās: Starptautiskie ceļojumi un tirdzniecība ir veicinājuši strauju DENV pārnesi pāri robežām, veicinot pāreju no ievestiem gadījumiem uz ilgstošu lokālu pārnesi. PVO uzraudzības dati liecina, ka laikā no 2010. līdz 2021. gadam Amerikas Savienotajās Valstīs tika ziņots par 7528 ar ceļošanu saistītiem denges drudža gadījumiem, no kuriem 3135 bija nepieciešama hospitalizācija un 19 gadījumos bija nāve.
(4) Vektoru izplatības paplašināšanās: Globālā mērogā Aedes aegypti un Aedes albopictus ģeogrāfiskais areāls turpina paplašināties, un Aedes odi arvien vairāk ieviešas Eiropas daļās. Līdz ar to denges drudzis ir attīstījies no tradicionāli reģionālas epidēmijas par globālu sabiedrības veselības apdraudējumu.
2.3 Vairāku serotipu kocirkulācijas un reinfekcijas mehānismi
Denges vīruss ietver četrus antigēniski atšķirīgus serotipus (DENV-1 līdz DENV-4). Infekcija ar vienu serotipu nodrošina ilgtermiņa aizsargājošu imunitāti pret šo specifisko serotipu, bet tikai īslaicīgu un daļēju krustenisko aizsardzību pret pārējiem trim serotipiem. Vispārējā populācija ir universāli uzņēmīga pret DENV, un tikai nelielai daļai inficēto indivīdu attīstās klīniska slimība [2].
Endēmiskos reģionos vairāki DENV serotipi bieži cirkulē vienlaicīgi, kā rezultātā indivīdiem dzīves laikā ir iespēja vairākkārt inficēties ar denges drudzi. PVO epidemioloģiskie pētījumi ir identificējuši vairāku serotipu kocirkulāciju kā galveno periodisku denges drudža uzliesmojumu virzītājspēku [1].
2.4 Sekundāra infekcija un no antivielām atkarīga pastiprināšanās
Kritiska un unikāla parādība denges drudža epidemioloģijā irantivielu atkarīga pastiprināšana (ADE)Sekundāras infekcijas laikā ar heterologu DENV serotipu primārās infekcijas laikā ražotās neneitralizējošās antivielas atvieglo vīrusa iekļūšanu monocītos un makrofāgos, tādējādi veicinot vīrusa replikāciju. PVO plaši atzīst šo mehānismu par galveno patogēno faktoru smagas denges drudža formas, tostarp denges hemorāģiskā drudža un denges šoka sindroma, gadījumā [1].
PVO epidemioloģiskie dati konsekventi liecina, ka personām ar sekundāru denges infekciju ir ievērojami lielāks risks saslimt ar smagu slimības formu salīdzinājumā ar personām ar primāro infekciju, un šī īpašība ir ļoti svarīga slimības uzraudzībai un klīniskajai pārvaldībai. Ir svarīgi atzīmēt, ka, lai gan sekundāras infekcijas laikā smagas slimības risks ir paaugstināts, infekcija ar jebkuru DENV serotipu var potenciāli progresēt līdz smagai denges formai [1].
2.5 Nespecifiskas klīniskās izpausmes un nepareizas diagnozes risks
Denges drudža klīniskās izpausmes ir ievērojami nespecifiskas, īpaši slimības sākumposmā, bieži vien pārklājoties ar citu odu pārnēsātu vīrusu infekciju (piemēram, čikungunjas un Zikas vīrusu), kā arī noteiktu elpceļu infekciju izpausmēm. PVO aplēses liecina, ka 40–80 % DENV infekciju ir asimptomātiskas [3].
Tipiskas klīniskās izpausmes ietver:
Akūts drudzis (ilgst 2–7 dienas, var būt divfāzīgs)
- Stipras galvassāpes un retroorbitālas sāpes (sāpes aiz acīm)
- Muskuļu un locītavu sāpes (parasti sauktas par "kaulu lūzuma drudzi")
-Makulas vai makulopapulāri izsitumi
- Vieglas hemorāģiskas izpausmes (piemēram, ekhimoze, deguna asiņošana, smaganu asiņošana)
Simptomātisku denges drudzi parasti iedala trīs atšķirīgās fāzēs: drudža fāzē, kritiskajā fāzē un atveseļošanās fāzē. Aptuveni mazāk nekā 5% pacientu ar simptomiem progresē līdz smagai denges formai. Specifisku klīnisko pazīmju trūkuma dēļ diagnozes noteikšana, pamatojoties tikai uz klīniskiem simptomiem, ir sarežģīta, kas palielina nepareizas un nepietiekamas diagnozes noteikšanas risku. PVO nepārprotami uzsver, ka klīniskā diagnoze vien nav pietiekama, lai nodrošinātu precizitāti, padarot laboratorisku apstiprinājumu neaizstājamu [1].
3 galvenie punkti no PVO dokumenta “Denges vīrusa laboratoriskā testēšana: pagaidu vadlīnijas, 2025. gada aprīlis”
2025. gada aprīlī Pasaules Veselības organizācija publicēja atjauninātas pagaidu vadlīnijas par DENV laboratorisko testēšanu, sniedzot autoritatīvus tehniskus norādījumus denges drudža diagnostikai globālā mērogā. Šīs vadlīnijas apkopo jaunākos pierādījumus par denges drudža laboratorisko testēšanu saistībā ar notiekošo globālo denges drudža ārkārtas situāciju un piedāvā praktiskus ieteikumus, kas pielāgoti vidēm ar dažādiem resursu līmeņiem.

3.1 Testēšanas stratēģijas pamatprincipi
Vadlīnijās uzsvērts, ka denges drudža diagnostikā jāizmanto kombinēta testēšanas stratēģija, kas balstīta uz slimības stadiju [1]. Ņemot vērā universāla diagnostikas algoritma trūkumu, testēšanas stratēģijas jāpielāgo vietējiem epidemioloģiskajiem apstākļiem, ņemot vērā šādus galvenos faktorus [1]:
-Infekcijas stadija: Vispiemērotāko testēšanas metodi nosaka dienu skaits pēc simptomu parādīšanās.
-Parauga veids: Pilnasiņu, plazmas vai seruma piemērotība DENV noteikšanai.
-Reģionālā epidemioloģija: lokāli cirkulējošie DENV serotipi un citu arbovīrusu līdzcirkulācija
-Koinfekcijas risks: Reģionos ar pārklājošu arbovīrusu cirkulāciju jāapsver vairāku testu veikšana, lai atšķirtu dažādus patogēnus.
3.2 Pakāpeniski balstīta testēšanas stratēģija
Saskaņā ar PVO vadlīnijām denges drudža laboratorijas testēšanai jāievēro skaidri laika intervāli, pamatojoties uz slimības stadiju [1,2]:
(1) Akūtās fāzes testēšana (≤7 dienas pēc saslimšanas sākuma)
-Nukleīnskābju testēšana (molekulārā testēšana): reversās transkripcijas polimerāzes ķēdes reakcija (RT-PCR) un citas molekulārās metodes ar augstu jutību atklāj DENV RNS.
-Antigēnu testēšana: NS1 antigēna noteikšana, kas kļūst nosakāms 1–3 dienu laikā pēc saslimšanas sākuma.
Akūtās fāzes laikā virēmijas līmenis ir relatīvi augsts, un nukleīnskābju un antigēnu testi sasniedz optimālu jutību.
(2) Atveseļošanās fāzes testēšana (≥4 dienas pēc saslimšanas sākuma)
-Seroloģiskā testēšana: IgM antivielas parasti kļūst nosakāmas aptuveni 4. dienā pēc saslimšanas sākuma.
Vairumā gadījumu IgM antivielas saglabājas 14–20 dienas, un dažos gadījumos saglabāšanās var ilgt līdz pat 90 dienām.
IgG testēšanai ir ierobežota vērtība akūta denges drudža diagnostikā iespējamo krustenisko reaktīvo antivielu dēļ no iepriekšējas flavivīrusa infekcijas vai vakcinācijas.
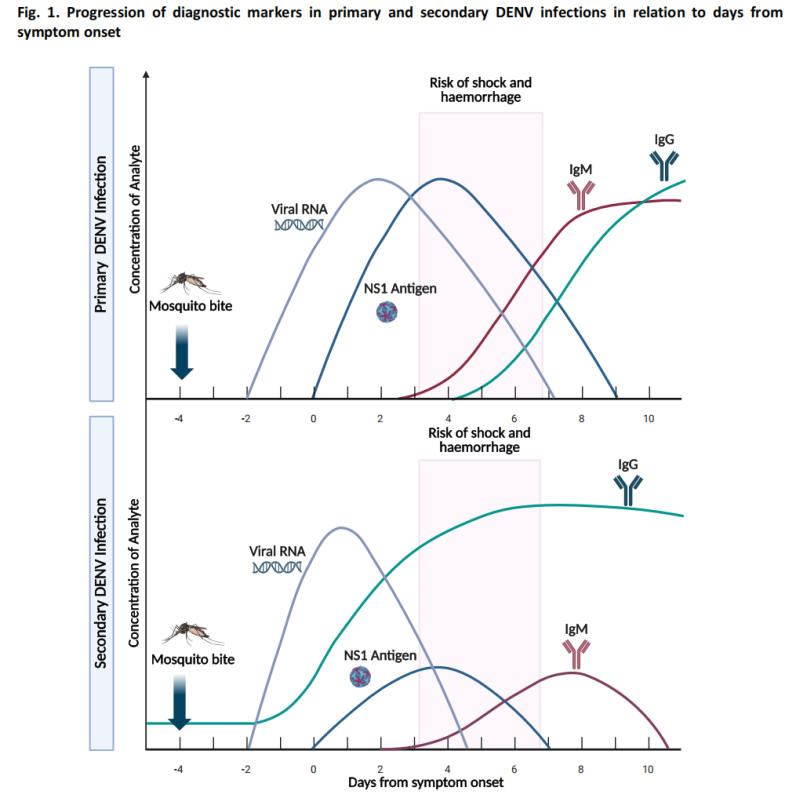
(3) Aizdomīgā gadījuma diagnostikas algoritms
Vadlīnijās ir iekļauts diagnostikas algoritms iespējamiem denges drudža gadījumiem, iesakot atbilstošas testēšanas metodes, pamatojoties uz dienām pēc simptomu parādīšanās: NS1 antigēna testēšana un nukleīnskābju testēšana ir galvenās pieejas agrīnā fāzē, savukārt seroloģiskā testēšana ir galvenā metode vēlīnā fāzē.
3.3 Testa metodes veiktspējas novērtēšana un izvēle
Saskaņā ar PVO datiem, dažādu denges drudža testēšanas veiktspējas un piemērojamo scenāriju sistemātisks novērtējums ir šāds:
| Testēšanas metode | Mērķis | Laika logs | Primārais pielietojuma scenārijs | Apsvērumi |
| Nukleīnskābju testēšana | Vīrusu RNS | 1–7 dienas pēc saslimšanas sākuma | Agrīna apstiprināšana, serotipa identifikācija | Zelta standarta metode; nepieciešams specializēts laboratorijas aprīkojums un tehniskās zināšanas |
| NS1 antigēna testēšana | Nestrukturāls proteīns | 1–3 dienas pēc saslimšanas sākuma | Agrīna ātra skrīninga | Pieejams ātrās diagnostikas testa (RDT) formātā, kas ir piemērots resursiem ierobežotiem apstākļiem |
| IgM antivielu testēšana | Specifiskas IgM antivielas | ≥4 dienas pēc saslimšanas sākuma | Nesenas infekcijas diagnoze | Viens seruma paraugs norāda tikai uz iespējamu nesenu infekciju; apstiprināšanai nepieciešama serokonversija. |
| IgG antivielu testēšana | Specifiskas IgG antivielas | Atveseļošanās/iepriekšēja infekcija | Epidemioloģiskā izmeklēšana, imunitātes statusa novērtēšana | Viens seruma paraugs nav piemērots akūtas denges drudža diagnostikai. |
| Kombinētā testēšana (NS1+IgM/IgG) | Antigēns + antivielas | Pilna slimības gaita | Denges infekcijas visaptveroša diagnostika | Pašlaik vislabāk funkcionējošais RDT formāts denges drudža diagnostikai |
| NGS | Vīrusu RNS | 1–7 dienas pēc saslimšanas sākuma | Vīrusu genoma uzraudzība | Nepieciešams specializēts sekvencēšanas aprīkojums un bioinformātikas analīzes iespējas |
4 Makro un mikro testu denges drudža noteikšanas produktu ieteikumi pēc scenārija
Lai atbalstītu denges drudža profilaksi un kontroli, Macro & Micro-Test nodrošina integrētu diagnostikas portfeli, kas aptver ātro skrīningu, molekulāro apstiprināšanu un genoma uzraudzību, apmierinot vajadzības dažādos uzliesmojumu pārvaldības posmos.
4.1 1. scenārijs: ātra skrīnings un mērķtiecīga uzraudzība
Attiecas uz drudža klīnikām, primārās veselības aprūpes iestādēm, uzliesmojuma kopienas skrīningu un ostas/robežas karantīnu.
Denges vīrusa NS1 antigēna eksprestests: atklāj agrīnu infekciju (1–3 dienas pēc saslimšanas sākuma) ar 15 minūšu rezultātiem ātrai triāžai.
-Denges vīrusa IgM/IgG antivielu tests: atšķir primārās/sekundārās infekcijas, lai novērtētu smagu slimības risku.
Denges vīrusa NS1 antigēna + IgM/IgG kombinētais eksprestests: vienlaikus nosaka antigēnu un antivielas pilnam diagnostikas kursam.
-Čikungunjas vīrusa IgM/IgG antivielu tests: ļauj veikt diferenciāldiagnozi ar denges drudzi, lai precīzi identificētu patogēnus.
4.2 2. scenārijs: precīza diagnostika un reaģēšana ārkārtas situācijā
-Denges vīrusa I/II/III/IV nukleīnskābju noteikšanas komplekts: atklāj un diferencē 4 serotipus (noteikšanas robeža 500 kopijas/ml) uzliesmojuma izsekošanai.
-Liofilizēts denges vīrusa PCR komplekts: pārvietojams istabas temperatūrā, piemērots resursiem ierobežotām vietām un pēkšņiem uzliesmojumiem.
-Dengue/Zika/Chikungunya Multiplex reāllaika PCR komplekts: Vienlaikus atklāj 3 arbovīrusus efektīvai diferenciāldiagnozei sarežģītu uzliesmojumu gadījumā.

Visi iepriekš minētie reaģenti ir saderīgi ar AIO 800 pilnībā automatizēto paraugu apstrādes sistēmu, samazinot manuālu darbību un savstarpēju piesārņojumu, kā arī uzlabojot efektivitāti un biodrošību.
4.3 3. scenārijs: genoma uzraudzība un vīrusu ciltsrakstu analīze
Attiecas uz valsts references laboratorijām, sabiedrības veselības pētniecības iestādēm, saskaņojot to ar PVO nostāju attiecībā uz NGS.
Macro & Micro-Test genoma uzraudzības risinājumi atbalsta pilna genoma sekvencēšanu vīrusu izsekošanai, pārnešanas ķēdes noskaidrošanai, variantu uzraudzībai un vakcīnas stratēģijas pielāgošanai. Tie atbalsta manuālas/automatizētas darbplūsmas, uzlabojot caurlaidspēju un reproducējamību, ļaujot laboratorijām pāriet no ikdienas testēšanas uz uzlabotu uzraudzību, kas atbilst PVO uzsvaram uz vīrusu evolūcijas uzraudzības stiprināšanu.

4.4 Integrētu risinājumu vērtība
Macro & Micro-Test nodrošina pilnīgus diagnostikas risinājumus arbovīrusu noteikšanai, atbalstot katru uzliesmojuma pārvaldības posmu: ātras skrīninga rīkus pirmās līnijas veselības aprūpes iestādēm, molekulāro apstiprināšanu precīzai diagnozei un visa genoma analīzes iespējas epidemioloģiskajai uzraudzībai. Ar augstas veiktspējas testiem, elastīgām darbplūsmām un automatizācijai gatavām platformām šie risinājumi dod iespēju laboratorijām un sabiedrības veselības sistēmām stiprināt sagatavotību un reaģēšanu uz jauniem arbovīrusu draudiem visā pasaulē.
Atsauces
[1] Pasaules Veselības organizācija. Denges vīrusa laboratoriskā testēšana: pagaidu vadlīnijas, 2025. gada aprīlis. Ženēva: Pasaules Veselības organizācija; 2025. gads.
[2] PVO Globālās arbovīrusu iniciatīvas tehniskā konsultatīvā grupa. Globālās sagatavotības un reaģēšanas uz arbovīrusu slimību draudiem stiprināšana: aicinājums rīkoties. Lancet Infect Dis. 2026;26(1):15–17.
[3] Lancet Microbe. Denges diagnostikas dilemmas pārvarēšana. Lancet Microbe. 2025;6(7):101190.
Publicēšanas laiks: 2026. gada 20. marts
